|
原代细胞培养原理 从供体取得组织,消化分离细胞后在体外进行的首次培养。一般使用酶法或机械处理法分离成大细胞,有时需要在合适的培养基中筛选出特定细胞。 用途 获得指定组织的单细胞。 基本操作流程 一、人或动物体内的组织分离获取,将其剪碎至1mm3的组织块,再采用如下方法进行原代细胞分离培养: 1 悬浮细胞的分离方法 将腹水、胸水、血液、羊水等悬液直接转至离心管中,1000rpm/分钟离心5min。去掉上清,离心沉淀用PBS清洗后1000rpm/min离心5分钟,重复两次。用培养基重悬,调整适当细胞浓度后分瓶培养。如选用悬液中某种细胞,可采用离心后的细胞分层液收获目的细胞,或者选用特殊标记抗体进行分选。 2 实体组织材料的分离方法 机械分散法:纤维成分很少的脑组织,部分胚胎组织,用剪刀剪碎至1mm3的组织块。用PBS清洗两次后,用吸管吹打,分散组织细胞或在不锈钢纱网内用钝物(注射器钝端)压挤使细胞从网孔中压挤出。收集细胞转入离心管中,1000rpm/分钟离心5min。去上清,加入含血清的培养基,重悬后移至培养瓶中培养。 消化分离法:细胞间质较少的软组织,如肝、肾、甲状腺、羊膜、胚胎组织、上皮组织等,用Hanks液清洗组织三次,剪成碎块大小为4mm左右,再用Hanks液洗2-3次以除去血球和脂肪组织,加入0.25%的胰蛋白酶,摇匀后放37℃培养箱孵育15min,再用Hanks液洗涤,弃去上清,共洗2-3次。加入少量含血清的培养基吹打分散,细胞计数,按适当的浓度分瓶培养。
二、原代细胞的传代、保存 传代:依椐细胞的生长状态,生长的细胞1:2或1:3进行传代。 保存:保存条件为DMSO+培养液+血清按比例添加;采用梯度降温的原则:室温→4℃(20分钟)→冰箱冷冻室(30分钟)→超低温冰箱(-80℃过夜)→液氮。
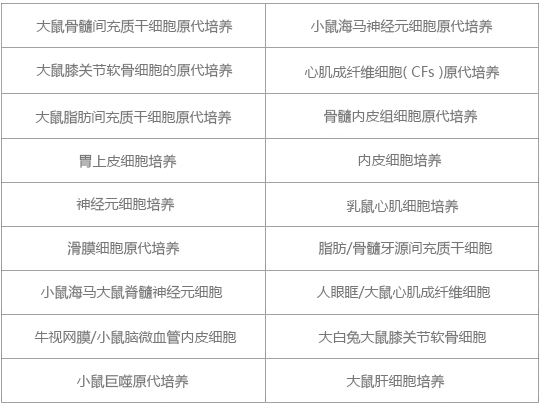
1 取出细胞,遵循快速溶解的原则,迅速放入37℃温水中快速解冻。 2 吸出细胞悬液,并加10倍以上培养液。 3 用培养液适当稀释后接种培养瓶,放入37℃、CO2培养箱静置培养。 注意事项 1 客户提供组织样本进行原代提取,必须要新鲜组织,并且 24h 内能送达我们实验室,注明组织来源,以及样本信息。 2 细胞培养一定要保持工作区的无菌清洁,先用紫外灯和臭氧杀菌1h ,然后通风30min,操作前需要换细胞间专用拖鞋,双手带上一次性橡胶手套并用75%乙醇消毒,穿上实验服,戴上一次性口罩和帽子,操作时不能大声说话,整个无菌操作都应该在酒精灯的周围进行。 我司平台已培养的原代细胞
实验室一瞥
实验价格/周期咨询
上一篇SD乳大鼠原代小胶质细胞培养下一篇SNP技术服务 |